In haar onderzoek aan de Vrije Universiteit Brussel (VUB) – Vlaams Instituut Biotechnologie (VIB) richtte biologe Jessie Vandierendonck zich op het ontwikkelen van nieuwe, alternatieve behandelingen om bacteriële infecties te bestrijden met behulp van (bacterio)fagen. Dat zijn virussen die bacteriën aanvallen en vernietigen. “Bacteriofagen werden al ontdekt vóór het eerste antibioticum, en we zien nu opnieuw hun enorme potentieel in de strijd tegen resistente bacteriën”, zegt Vandierendonck.
De wereldwijde opkomst van bacteriën die ongevoelig zijn geworden voor antibiotica vormt een groeiende bedreiging voor de volksgezondheid. Omdat klassieke antibiotica steeds minder goed werken, is er dringend nood aan nieuwe manieren om bacteriële infecties te bestrijden. Eén van de bacteriën die door de Wereldgezondheidsorganisatie als “kritiek” wordt beschouwd in de zoektocht naar nieuwe behandelingen, is Escherichia coli. Die darmbacterie is meestal onschadelijk, maar bepaalde varianten kunnen ernstige infecties veroorzaken, zoals darminfecties, urineweginfecties en bloedvergiftiging.
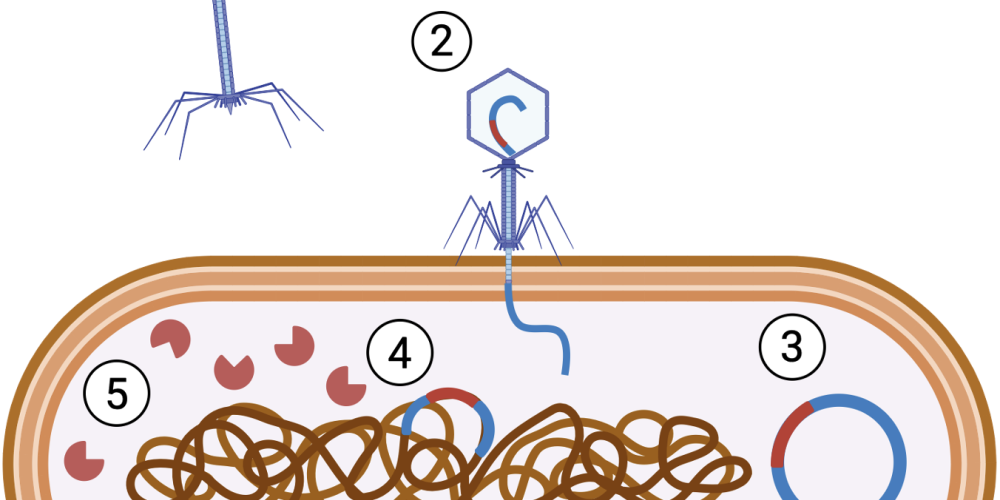
Je kan een bacteriofaag vergelijken met een soort maanlander die zich vasthecht aan specifieke bacteriën met behulp van bacteriële receptoren aan de celwand. Eens vastgehecht aan de bacterie zal de faag zijn genetisch materiaal injecteren in deze gastheer. Dan zijn er twee opties om zichzelf te reproduceren, ofwel maakt de bacteriofaag gebruik van de bacteriële “fabriekjes” om nieuwe fagen aan te maken die uiteindelijk de bacteriecel doen openbarsten en doden, ofwel deelt het genetisch materiaal van de “getemperde” faag mee met bacteriecellen in een sluimerende toestand. Dat eerste maakt bacteriofagen een interessant en natuurlijk hulpmiddel om bacteriën gericht te gaan doden als alternatief voor antibiotica. Getemperde fagen daarentegen doden de bacteriecellen niet per se en hier is Vandierendoncks onderzoek op gericht.
Naast faagtherapie onderzocht ze ook het gebruik van bacteriële toxine-antitoxinesystemen, die bestaan uit een toxine dat celdood veroorzaakt en een antitoxine dat die werking tegengaat. Door fagen en toxines te combineren, werkte Jessie aan een innovatieve methode om pathogene E. coli-bacteriën aan te pakken. In haar onderzoek werden getemperde fagen genetisch gemodificeerd zodat ze bacteriële toxines kunnen overdragen aan schadelijke bacteriën. Eenmaal binnen in de bacteriële cel wordt het toxine tot expressie gebracht, waardoor de bacterie effectief wordt uitgeschakeld. “Door fagen te gebruiken als transportmiddel voor toxines kunnen we zeer gericht te werk gaan, wat het risico op schade aan gezonde bacteriën vermindert in tegenstelling tot klassieke antibiotica”, legt Vandierendonck uit.
Het genetisch manipuleren van toxine-dragende fagen bleek echter niet eenvoudig, omdat het klonen van toxine genen de groei van de bacteriële gastheercellen kan stoppen. Om dat probleem te omzeilen, ontwikkelde Jessie nieuwe kloneringsstrategieën waarbij de expressie van de toxines op verschillende niveaus wordt gecontroleerd. Ze isoleerde bovendien fagen uit enterohemorragische E. coli, en karakteriseerde deze zowel genetisch als morfologisch, inclusief de identificatie van de bacteriële receptoren waaraan ze zich hechten voor infectie. Als bewijs van concept combineerde ze een van deze fagen met toxinegenen en toonde ze in het laboratorium aan dat deze recombinante faag de doelwitbacterie effectief kon doden via het toxine.
Jessie behaalde in 2020 haar master in de biologie aan de VUB en startte daarna haar doctoraat in de onderzoeksgroep Structurele Biologie Brussel, onder leiding van prof. dr. ir. Remy Loris. Tijdens haar doctoraat publiceerde ze twee wetenschappelijke artikelen als eerste auteur, begeleidde ze masterstudenten en nam ze deel aan verschillende internationale conferenties over bacteriofagen. “We hopen dat dit onderzoek een stap vooruit betekent in de ontwikkeling van gerichte, duurzame en veilige behandelingen tegen multiresistente bacteriën,” besluit Jessie.